いま、ここで、すぐ知りたい、伝えたい
リ ア ル タ イ ム P C R 検査をもっと身近に、簡単に





Suggesting Updated New Bacterial Clusters (GF-MoR Complexes) for
Periodontal and Peri-Implant Diseases and Conditions.Microorganisms
(2024); 12(11):2214.
悪玉3菌の迅速スクリーニングを実現
個別検査にも対応



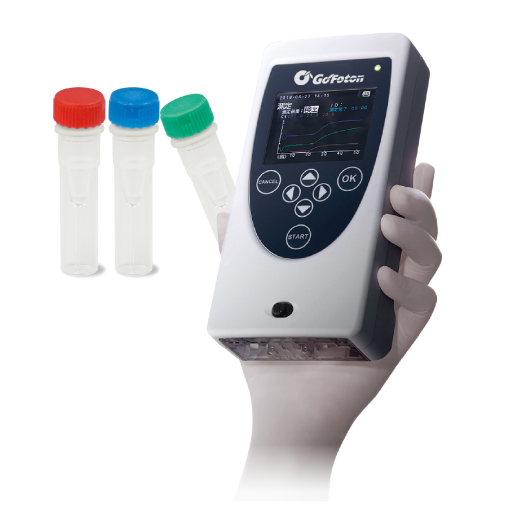
臨床現場即時検査を可能にしたPCR装置。
マイクロ流路で試料が高温・低温間を往復する独自の温度制御法により、
サイズダウン・低消費電力・高速化を実現。

| 項目 | 仕様 |
|---|---|
| 装置名 | PicoGene PCR1100 |
| 本体サイズ | 200×100×50mm |
| 重量 | 約560g |
| 電源 | 100-240V 50/60Hz(ACアダプター付属) 5V3A(USB給電ケーブル付属) |
| サンプル数 | 1 |
| 測定チップ | 76×26×3mm(別売) |
| 項目数 | 最大3項目 |
| インターフェイス | Bluetooth®(Ver3以降) ※PCと接続可能 専用USBメモリー付属 |
| 対応OS | Windows® 10(32bit/64bit)Windows® 11(32bit/64bit) |
| 付属品 | CD-ROM(PCソフトウエア等)、クイックスタートマニュアル、ACアダプター、USB給電ケーブル |
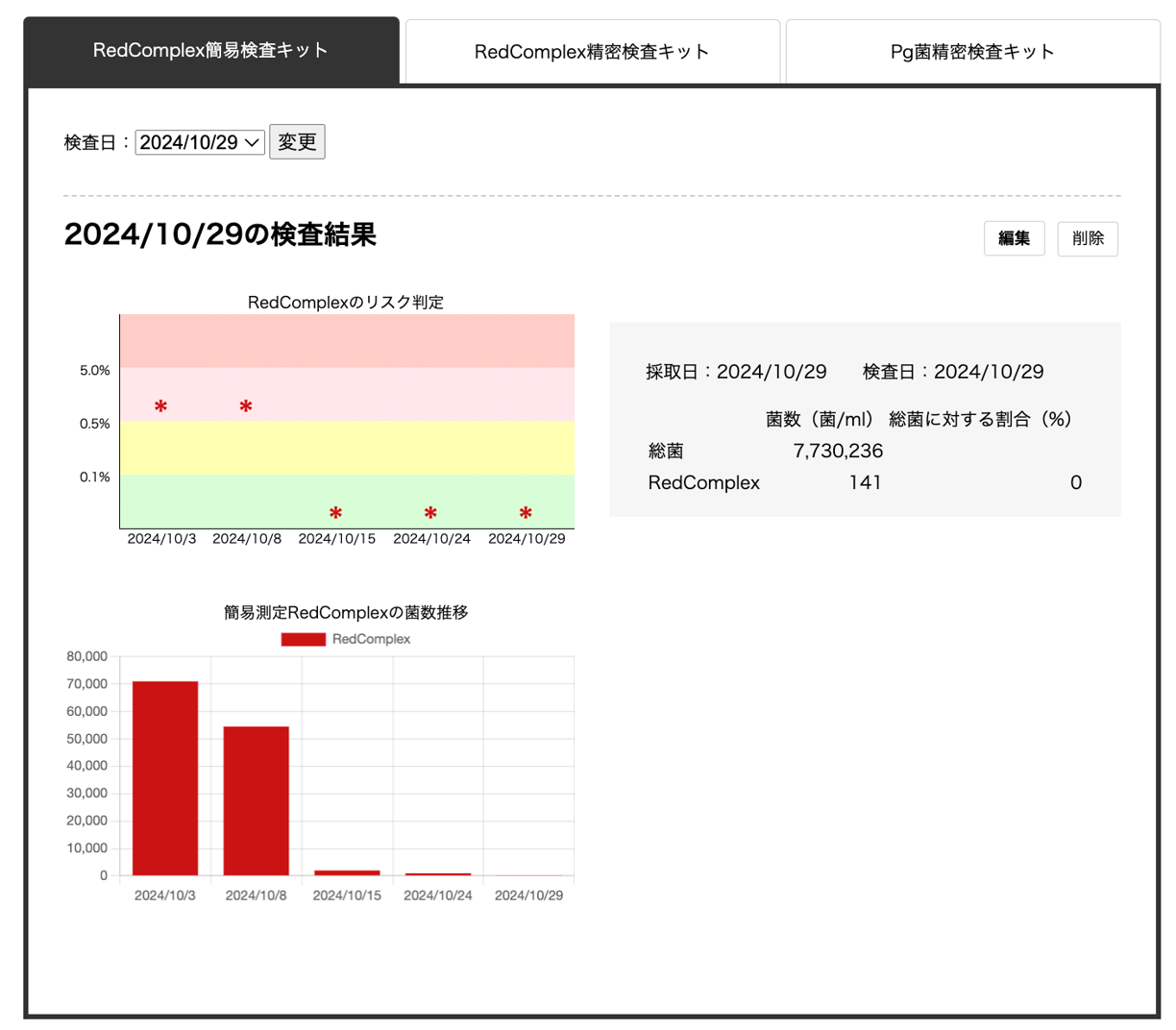
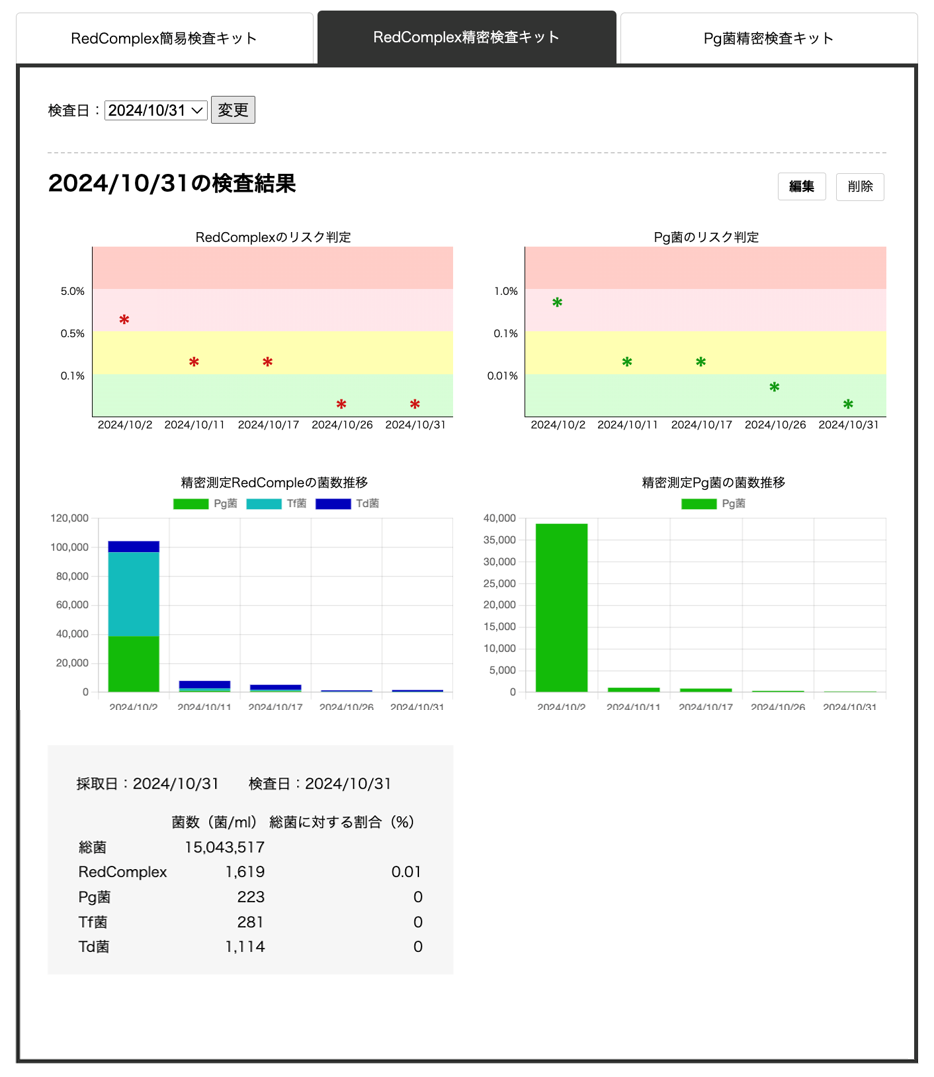
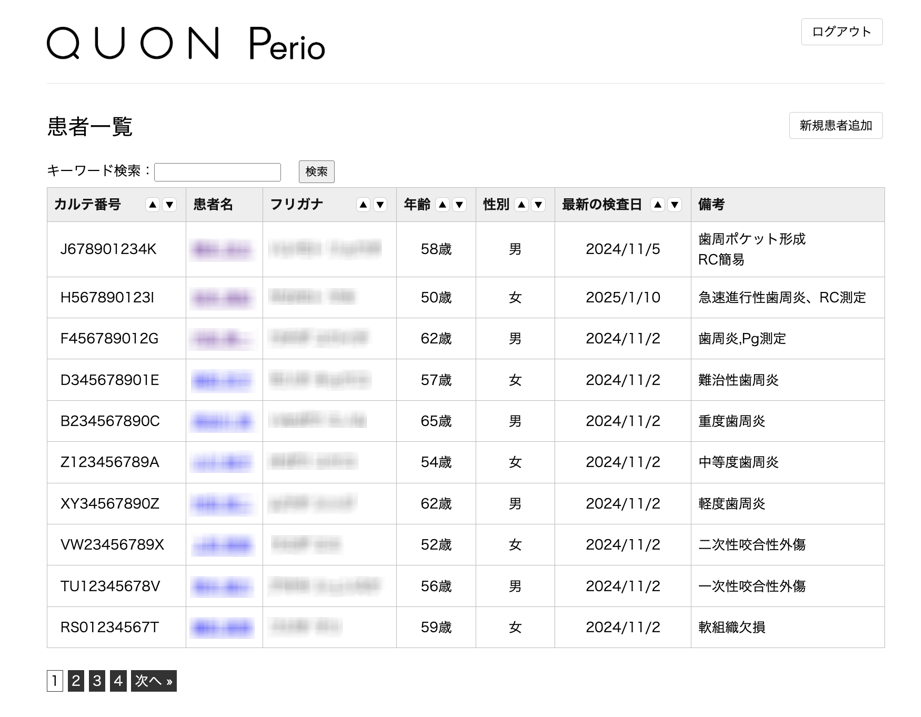
過去の検査データとの比較や患者向け説明資料の出力も可能なクラウドシステム
判定基準は以下の通り。なおハイミドルリスクは、ガイドラインの他の判定基準から推定し、iCATが独自に設定。
| ハイリスク | ハイミドルリスク | ミドルリスク | ローリスク | |
|---|---|---|---|---|
| red complex | 5%以上 | 0.5%~5% | 0.1%〜0.5% | 0.1%以下 |
| Pg菌 | 1%以上 | 0.1%~1% | 0.01%〜0.1% | 0.01%以下 |
2つのエビデンスとして、(1)red complex3菌の合成DNAによるQUON Perioの精度を示すエビデンスと、(2)純培養されたred complex3菌をヒトだ液に混ぜ、QUON Perioと高精度なリアルタイムPCRとの比較検証のエビデンスを示す。
エビデンス1.合成DNAによる検証
概要
red complexの3菌(Pg菌、Td菌、Tf菌)のDNAを滅菌水にて段階希釈。既知のDNAコピー数(菌量:cell/ml)の試料を作製。QUON PerioによるリアルタイムPCRを実施。蛍光シグナルが閾値に達するサイクル数(Ct値)を各濃度で計測することで検量線を作成。QUON PeiroのリアルタイムPCRシステムの相関係数(R2値)が1.0に近く直線性であることから、高い定量性を有することが示された。
- Ct値:Threshold Cycle(サイクル閾値)。反応の蛍光シグナルがThreshold Lineと交差する時点のサイクル数。DNAの初期コピー数の算出に使用できる。
- 検量線:既知濃度の段階希釈物を使用し、実験試料中のターゲットテンプレートの初期開始量を決定することで、菌量を求めることが出来る。
- 相関係数(R2):R2値は検量線の直線性を反映し、データの精度指標。R2値は1に近い値(直線性)が良好な数値。
<参考>
材料と方法
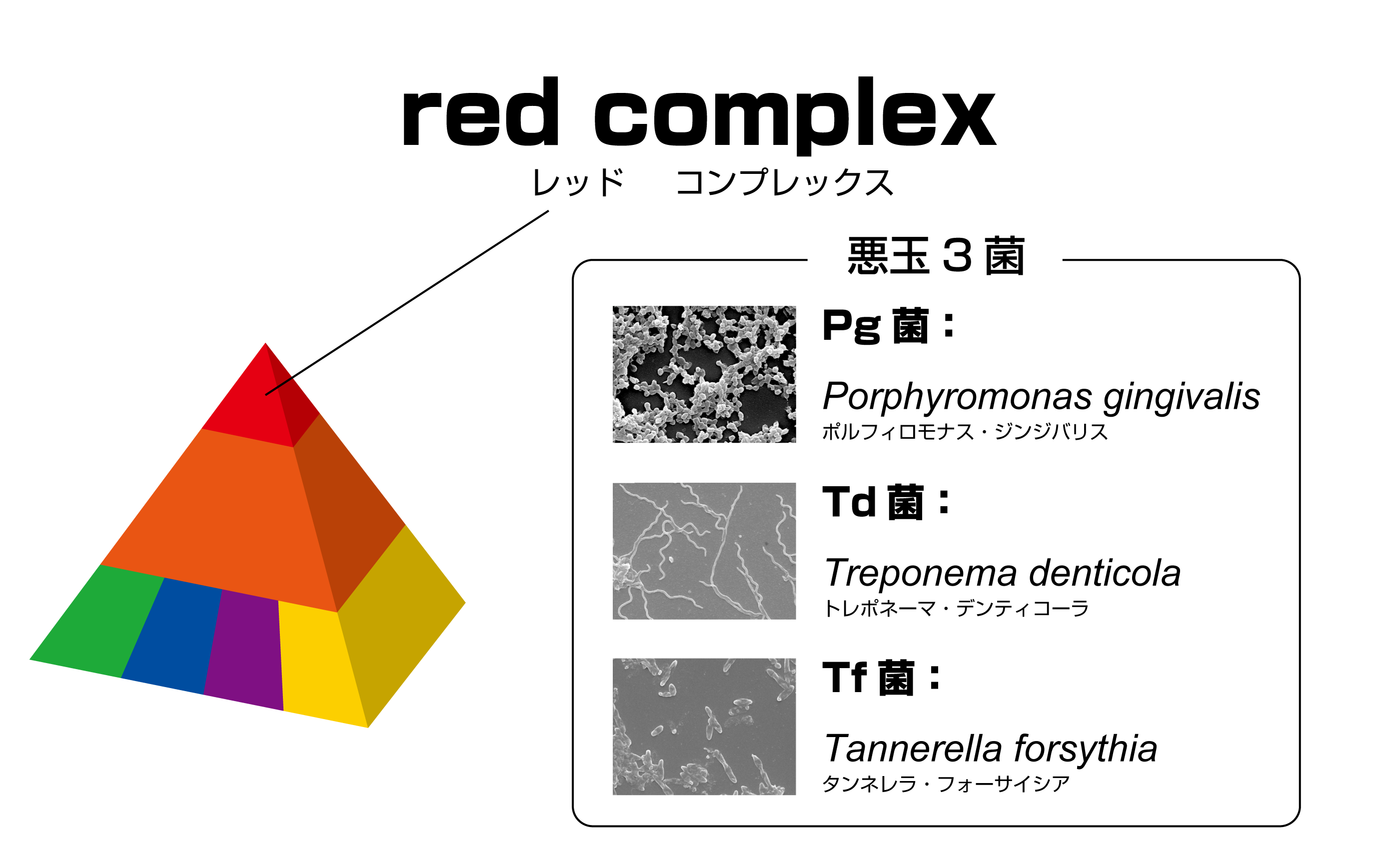
- DNA:red complexの3菌(Pg菌、Td菌、Tf菌)のDNAを購入
- 試料:購入業者のプロトコルに従って滅菌水にて段階希釈し、既知のDNAコピー数(菌量:cell/ml)の試料を作製。
- 計測:QUON Perioの試薬である①red complexをまとめて簡易的に計測する「簡易検査キット」と、② red complexを個別で精密に計測する「精密検査キット 」の各々を用いて、 QUON Perioの装置によるリアルタイムPCRを実施。
- 検量線:蛍光シグナルが閾値に達するサイクル数(いわゆるCt値)を各濃度で計測。検量線を作成し、相関係数を求めた。
結果
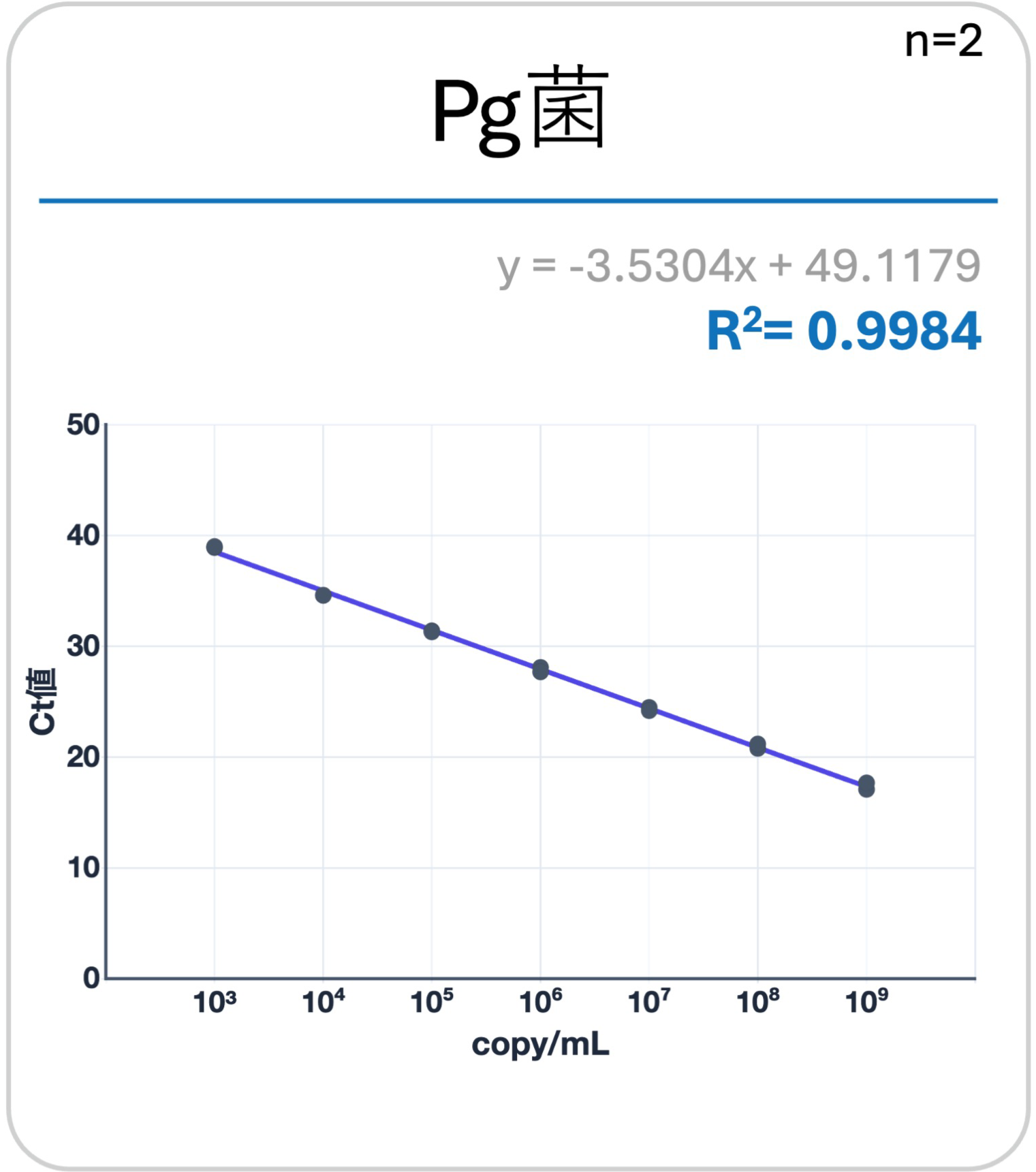
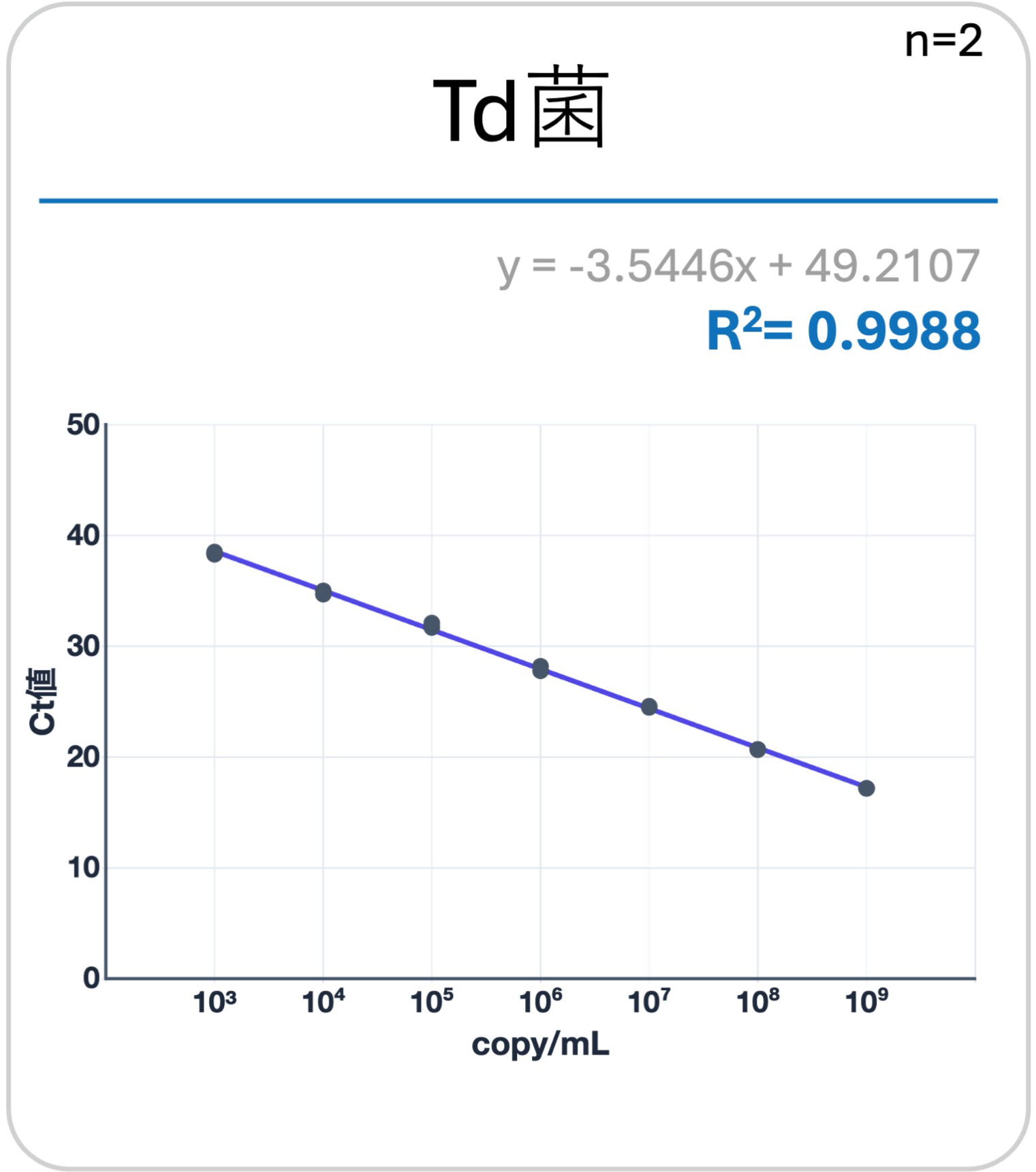
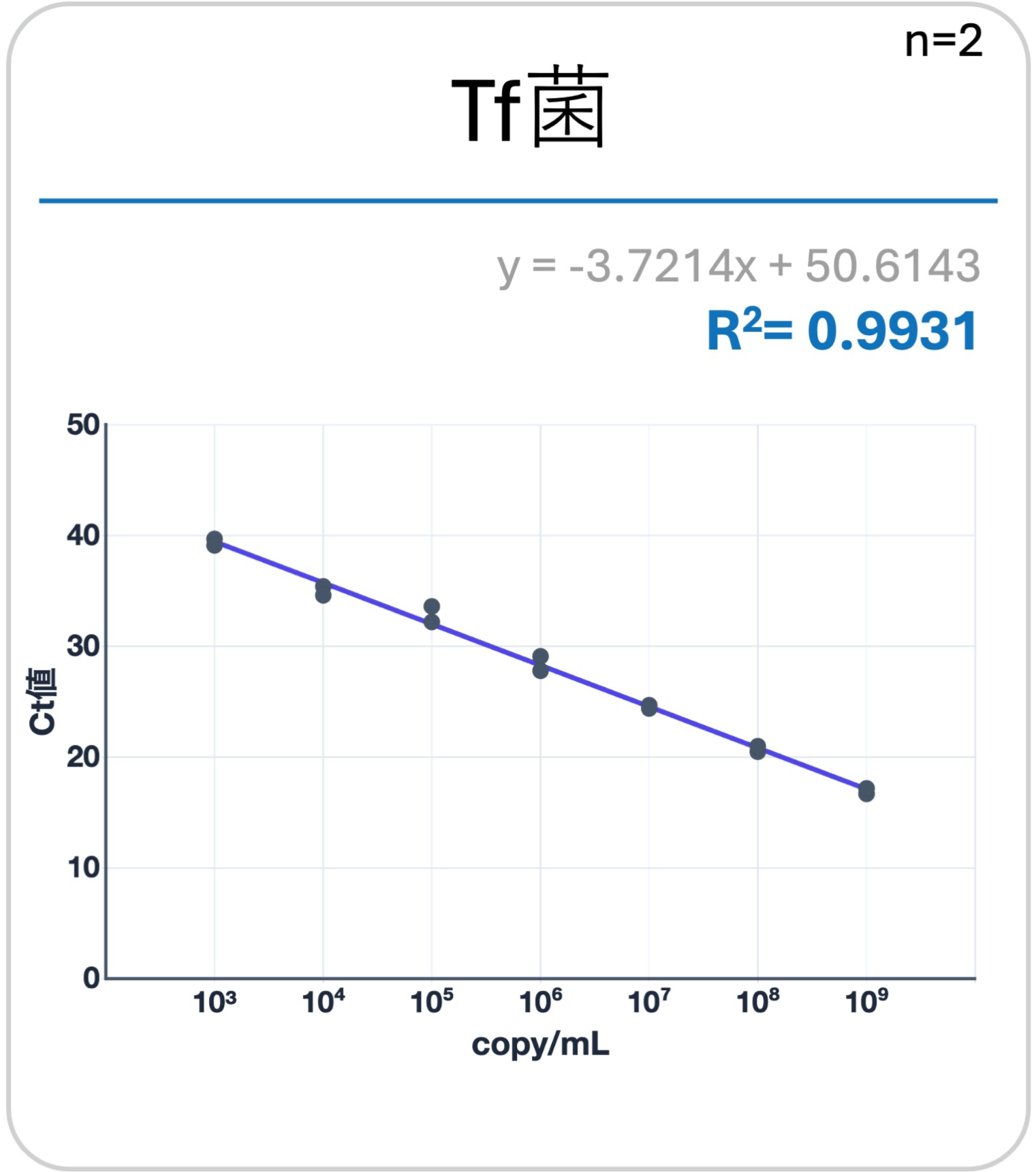
リアルタイム全てのred complexの3菌(Pg菌、Td菌、Tf菌)において、相関係数(R2値)が1.0に近い値を示した(直線性を示した)。
① 簡易検査キット(3菌まとめて)
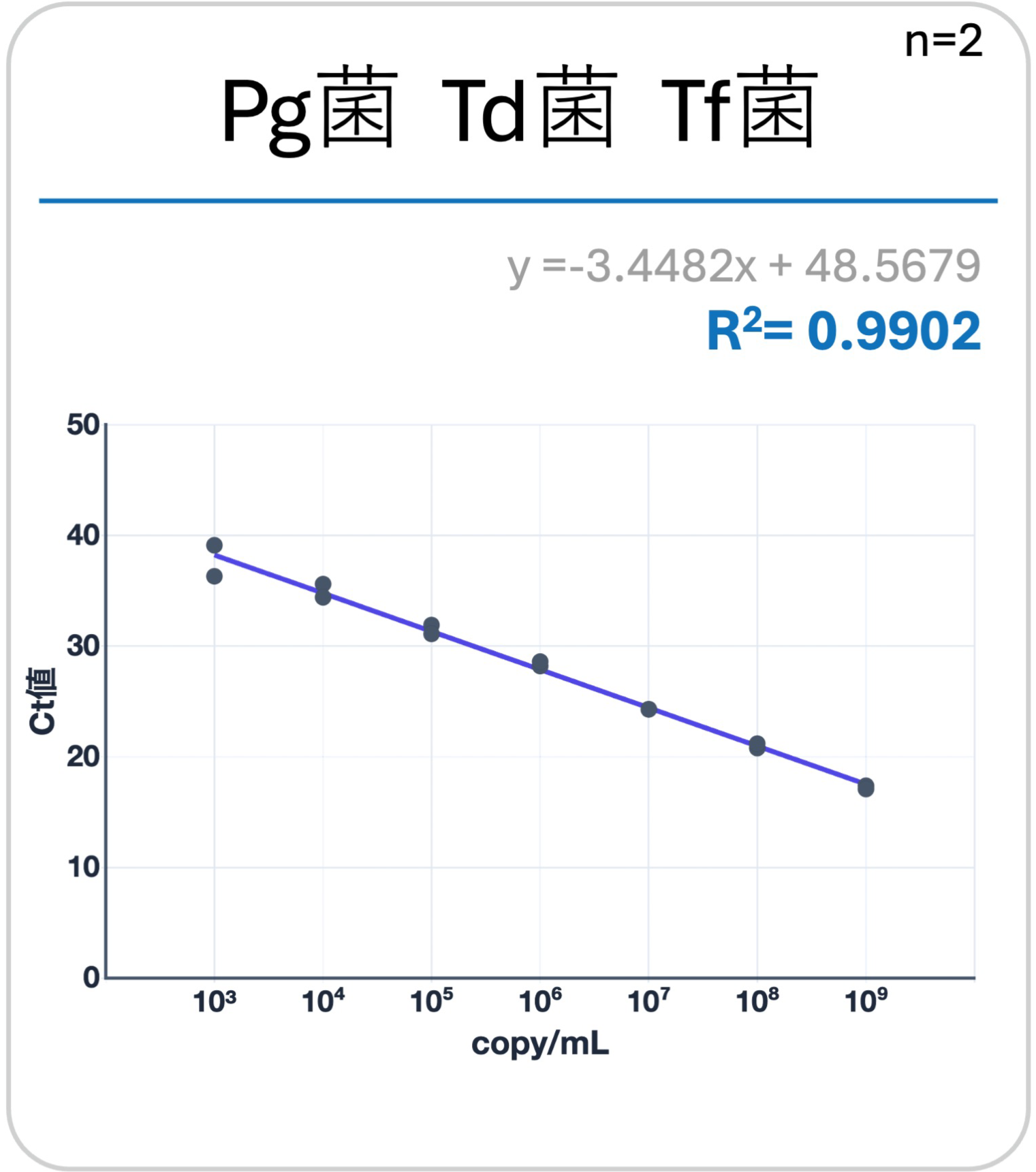
② 精密検査キット(3菌個別で)
結論
QUON Perioの「簡易検査キット」ならびに「精密検査キット」が、red complexの3菌(Pg菌、Td菌、Tf菌)において精度高く計測できることがわかった。
エビデンス2.培養菌/ヒトだ液による高精度リアルタイムPCRとの比較検証
概要
純培養したred complex3菌(Pg菌、Td菌、Tf菌)を「ヒトだ液」にて段階希釈。既知の菌量(cfu/チューブ)の試料を作製。QUON PerioによるリアルタイムPCRと、大阪大学大学院歯学研究科 予防歯科学講座の研究で用いられている高精度なリアルタイムPCRシステム(装置:Rotor-Gene Q、QIAGEN社)と、検量線の直線性を比較検証。結果、 QUON Perioのシステムが高精度なリアルタイムPCRシステムと同等の高い精度を示すことがわかった。
材料と方法
- 培養菌:大阪大学大学院歯学研究科 予防歯科学講座で純培養されたred complexの3菌(Pg菌、Td菌、Tf菌)
- 試料:red complex 3菌種を保有しない「ヒトだ液」(夾雑物を想定)で段階希釈し、既知の菌量(cfu/チューブ)に調整。
- 計測:QUON PerioによるリアルタイムPCRと、同講座の臨床研究を含む基礎研究で用いられている高精度なリアルタイムPCRシステム(装置:Rotor-Gene Q、QIAGEN社)によるリアルタイムPCRを実施。
- 検量線:両システムにおける各濃度でのCt値を計測。各々検量線を作成し、相関係数を求め比較した。
結果
QUON Peiroの相関係数(R2値)は、高精度なリアルタイムPCRシステムと比較して同等の高値を示した。

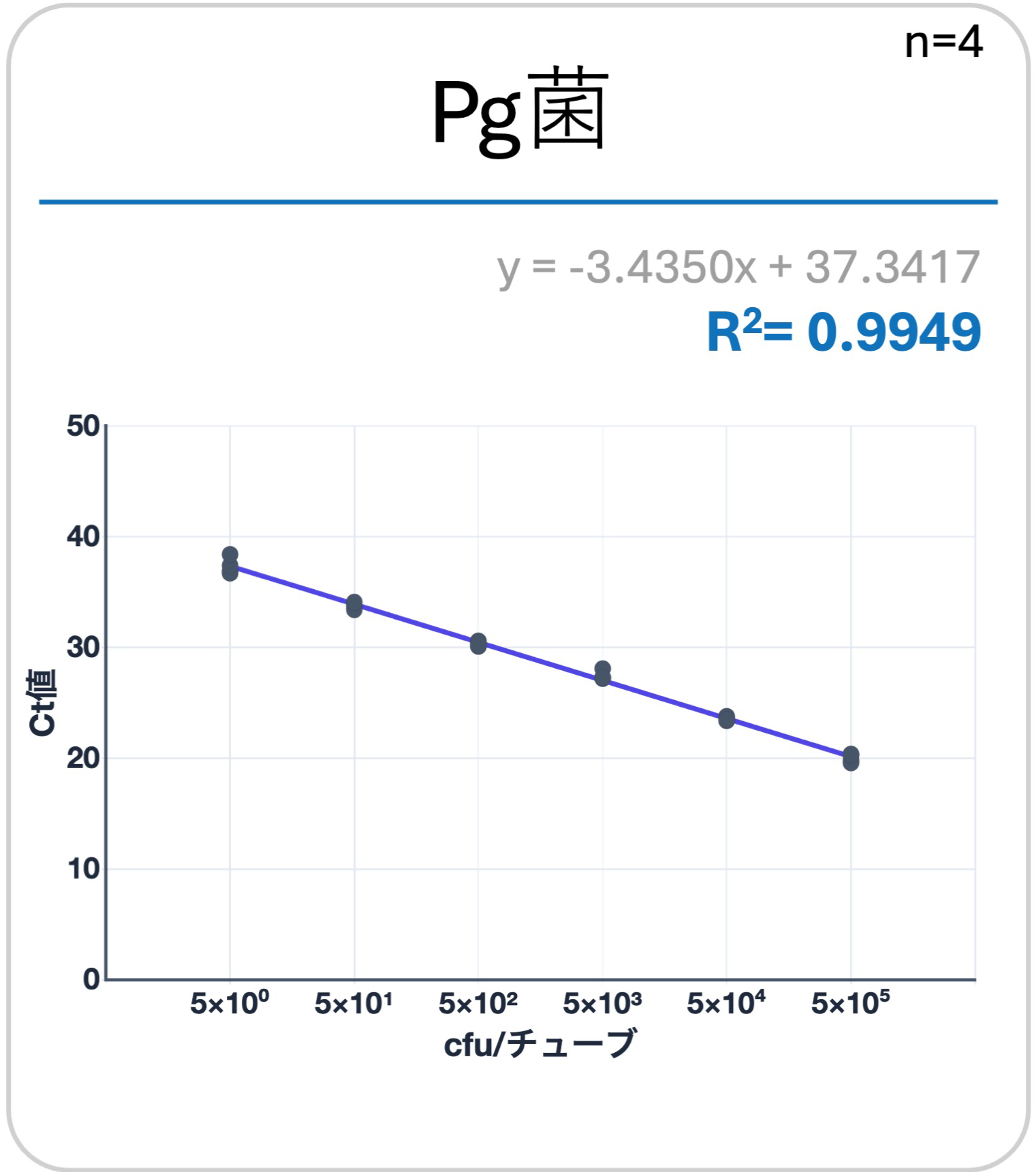
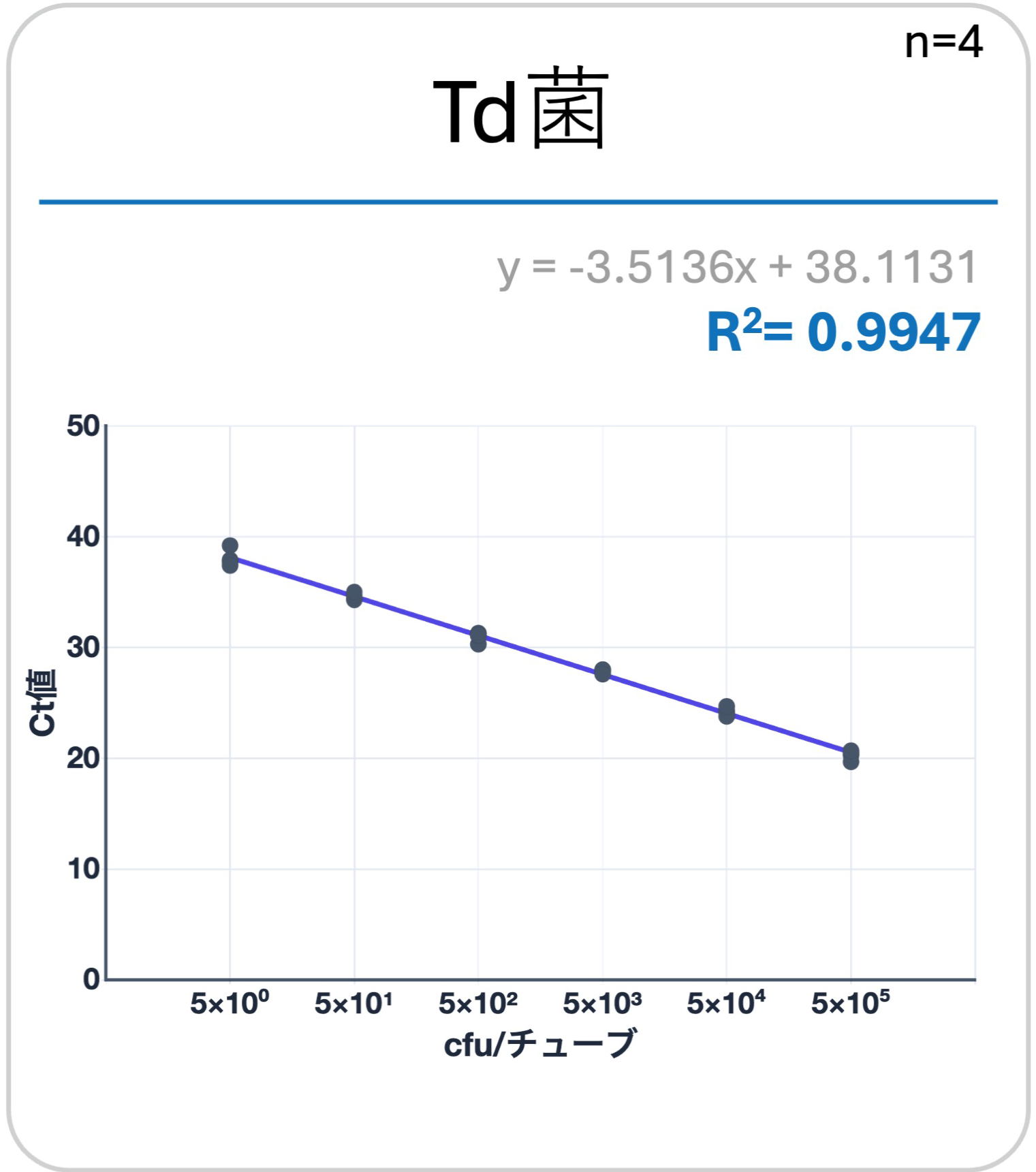
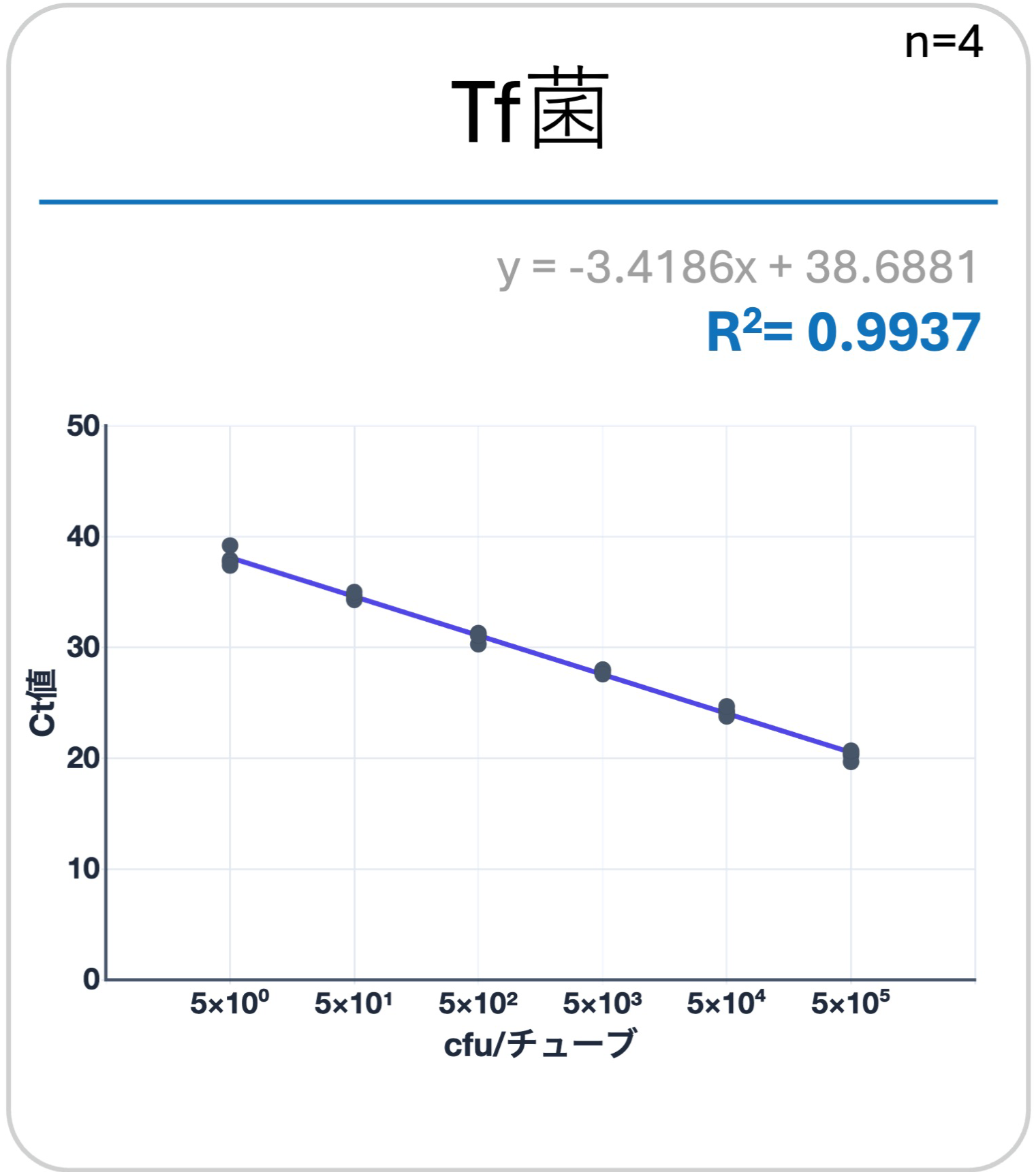

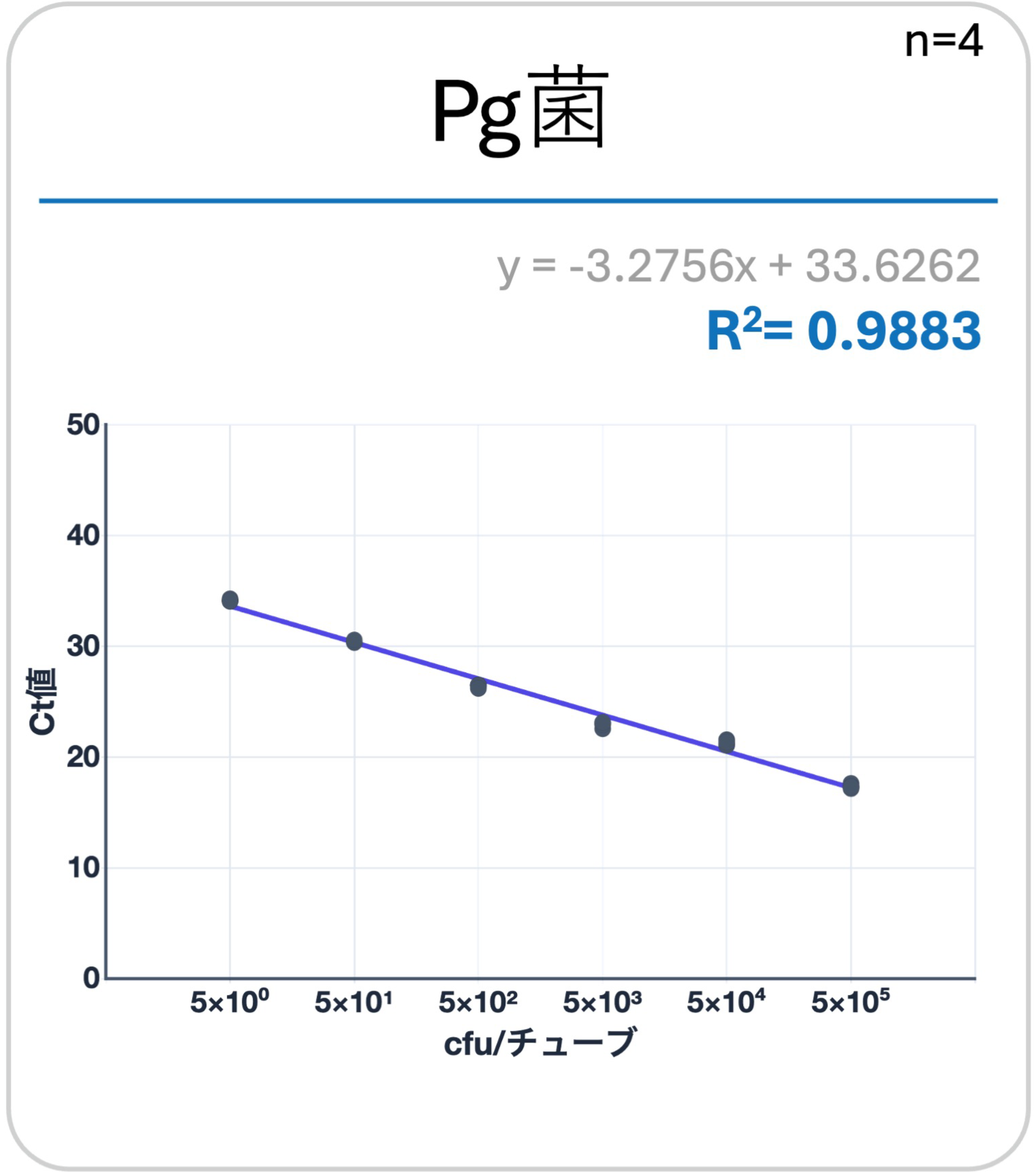
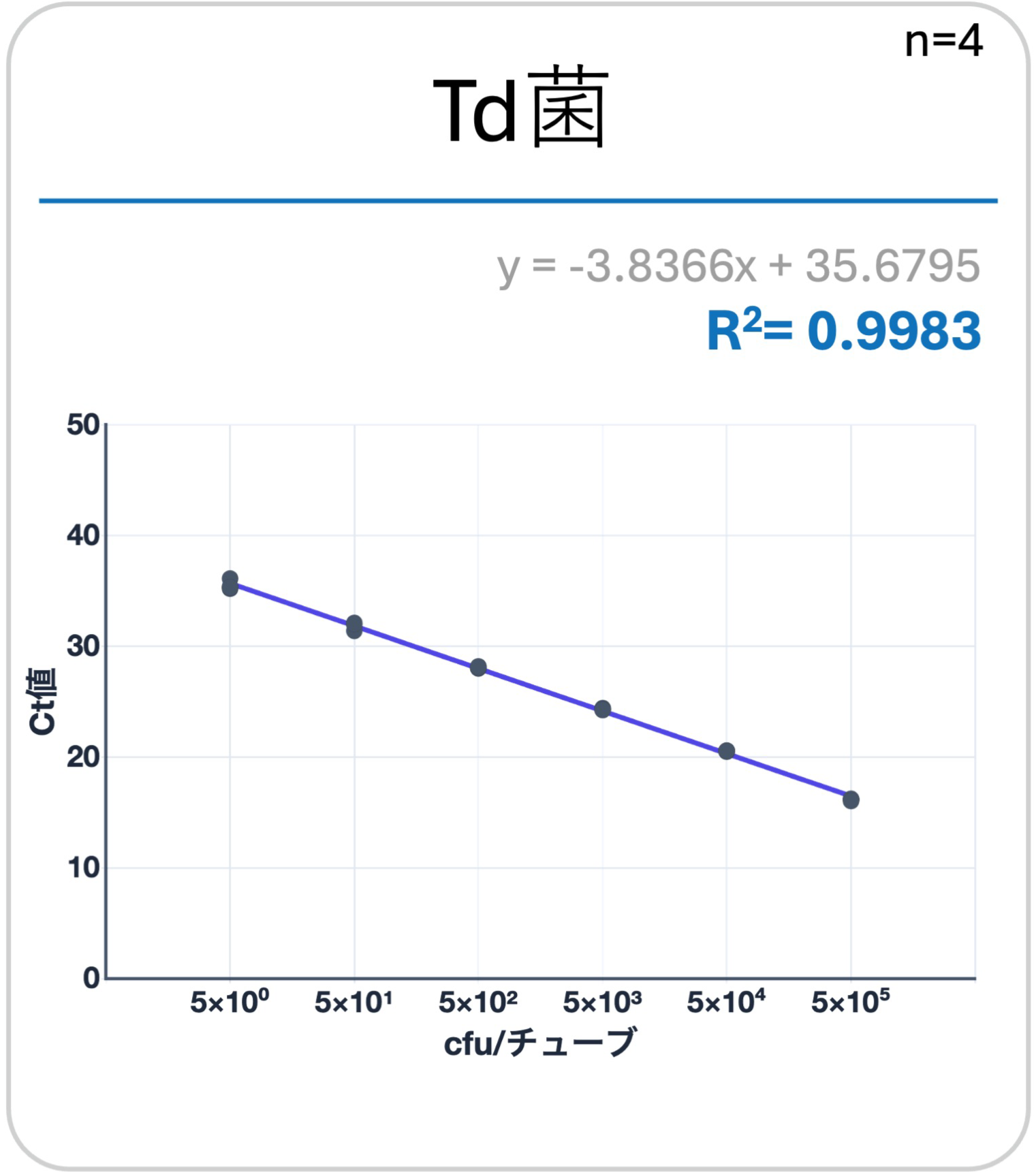
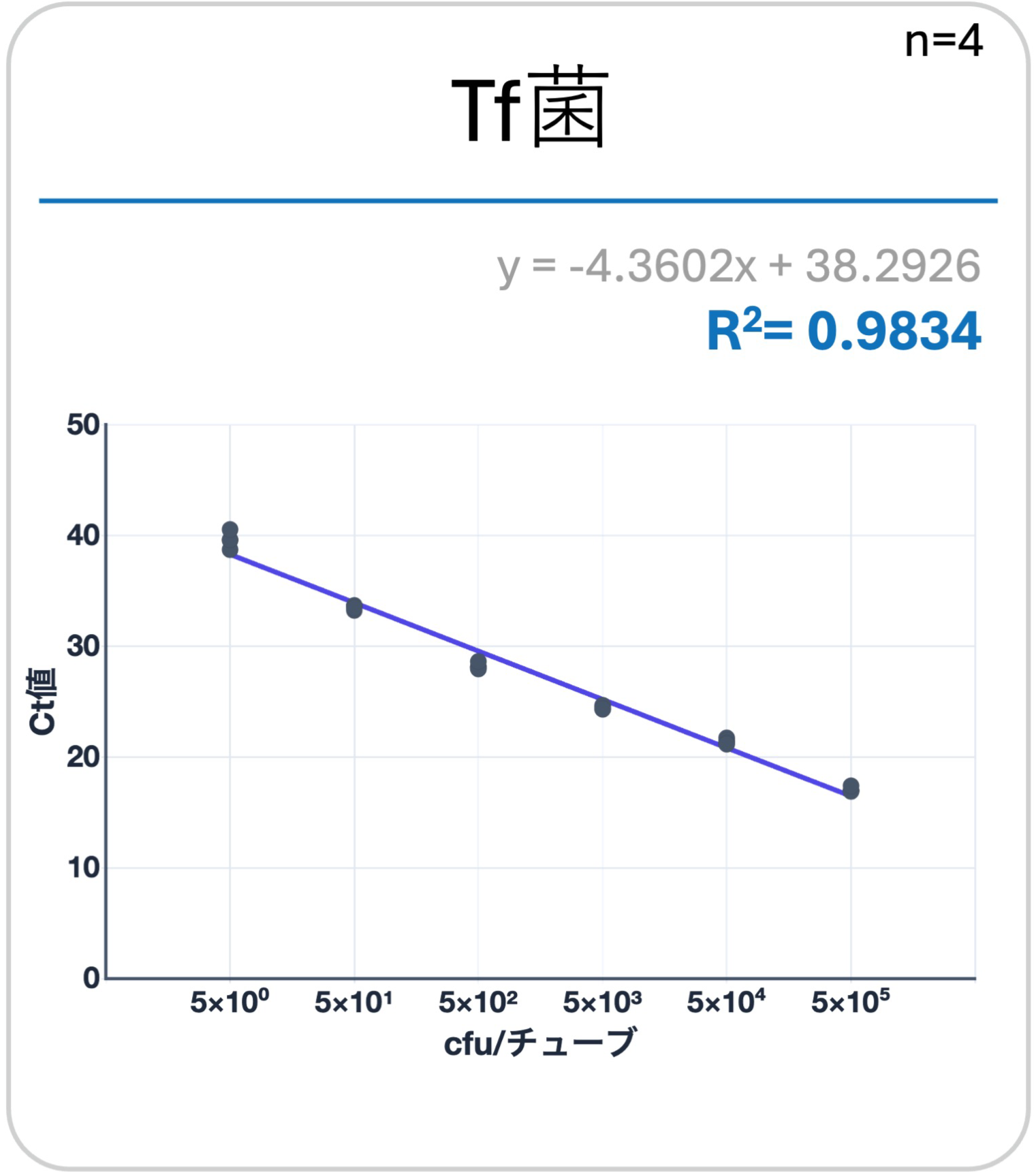
結論
QUON Perioの「簡易検査キット」ならびに「精密検査キット」が、red complexの3菌(Pg菌、Td菌、Tf菌)において精度高く計測できることがわかった。
ご使用時には、試薬容器のフタ側を持ち、遠心力で中身すべてを容器底へ振り落としてからご使用ください。

ただし、採取した検体をフィルターチップで吸引する際には、検体の泡がフィルターチップ内に入らないよう注意して吸引してください。